Apa itu aromatisasi minyak? Tuliskan persamaannya. Ciri-ciri umum minyak
1. Apa yang utama? mata air alami hidrokarbon tahukah anda?
Minyak, gas alam, serpih, batu bara.
2. Bagaimana komposisinya gas alam? Arahkan ke peta geografis simpanan terpenting: a) gas alam; mendidihkan; c) batubara.
3. Apa kelebihan gas alam dibandingkan bahan bakar lainnya? Untuk tujuan apa gas alam digunakan? industri kimia?
Gas alam, dibandingkan dengan sumber hidrokarbon lainnya, merupakan gas yang paling mudah diproduksi, diangkut, dan diproses. Dalam industri kimia, gas alam digunakan sebagai sumber hidrokarbon dengan berat molekul rendah.
4. Menulis persamaan reaksi memperoleh: a) asetilena dari metana; b) karet kloroprena dari asetilena; c) karbon tetraklorida dari metana. 
5. Apa perbedaan antara gas minyak bumi dan gas alam?
Gas terkait adalah hidrokarbon yang mudah menguap yang dilarutkan dalam minyak. Isolasi mereka terjadi dengan distilasi. Tidak seperti gas alam, gas ini dapat diisolasi pada setiap tahap pengembangan ladang minyak.
6. Jelaskan produk utama yang diperoleh dari gas minyak bumi terkait.
Produk utama: isomer metana, etana, propana, n-butana, pentana, isobutana, isopentana, n-heksana, n-heptana, heksana, dan heptana.
7. Sebutkan produk minyak bumi yang paling penting, sebutkan komposisinya dan area penerapannya. 
8. Minyak pelumas apa yang digunakan dalam produksi?
Oli motor, transmisi, industri, emulsi pelumas dan pendingin untuk mesin pemotong logam, dll.
9. Bagaimana cara penyulingan minyak? 
10. Apa yang dimaksud dengan perengkahan minyak bumi? Tuliskan persamaan reaksi pembelahan hidrokarbon ![]() Dan
Dan ![]() dalam proses ini.
dalam proses ini. 
11. Mengapa bensin dapat diperoleh tidak lebih dari 20% dengan penyulingan minyak secara langsung?
Pasalnya, kandungan fraksi bensin dalam minyak bumi terbatas.
12. Apa perbedaan perengkahan termal dengan perengkahan katalitik? Berikan karakteristik bensin perengkahan termal dan katalitik.
Dalam perengkahan termal, reaktan perlu dipanaskan suhu tinggi, dengan katalitik - pengenalan katalis mengurangi energi aktivasi reaksi, yang memungkinkan penurunan suhu reaksi secara signifikan.
13. Bagaimana cara membedakan bensin retak dan bensin sulingan murni?
Bensin cracking memiliki angka oktan yang lebih tinggi dibandingkan dengan bensin sulingan lurus, yaitu. lebih tahan terhadap ledakan dan direkomendasikan untuk digunakan pada mesin pembakaran internal.
14. Apa yang dimaksud dengan aromatisasi minyak? Tulis persamaan reaksi yang menjelaskan proses ini.

15. Apa produk utama yang diperoleh dari batubara kokas?
Naftalena, antrasena, fenantrena, fenol dan minyak batubara.
16. Bagaimana kokas diperoleh dan di mana digunakan?
Kokas adalah produk padat, berpori, berwarna abu-abu yang diperoleh dari batubara kelapa pada suhu 950-1100 tanpa oksigen. Ini digunakan untuk peleburan besi cor, sebagai bahan bakar tanpa asap, zat pereduksi bijih besi, penghancur untuk bahan batch.
17. Produk utama apa yang diterima:
a) dari tar batubara; b) dari air tar; c) dari gas oven kokas? Dimana mereka digunakan? Yang bahan organik dapatkah diperoleh dari gas coke oven?
a) benzena, toluena, naftalena – industri kimia
b) amonia, fenol, asam organik – industri kimia
c) hidrogen, metana, etilen - bahan bakar.
18. Ingat semua metode utama memperoleh hidrokarbon aromatik. Apa perbedaan metode produksi hidrokarbon aromatik dari produk batubara kokas dan minyak? Tuliskan persamaan reaksi yang bersangkutan.
Mereka berbeda dalam metode produksinya: penyulingan minyak primer didasarkan pada perbedaan sifat fisik berbagai fraksi, dan kokas murni didasarkan pada sifat kimia batubara.
19. Jelaskan bagaimana proses penyelesaiannya masalah energi Negara ini akan memperbaiki cara pengolahan dan penggunaan sumber daya hidrokarbon alami.
Pencarian sumber energi baru, optimalisasi produksi minyak dan proses penyulingan, pengembangan katalis baru untuk mengurangi biaya keseluruhan produksi, dll.
20. Bagaimana prospek penerimaannya bahan bakar cair dari batu bara?
Di masa depan, produksi bahan bakar cair dari batu bara bisa dilakukan asalkan biaya produksinya bisa ditekan.
Soal 1. Diketahui gas tersebut mengandung fraksi volume 0,9 metana, 0,05 etana, 0,03 propana, 0,02 nitrogen. Berapa volume udara yang diperlukan untuk membakar 1 m3 gas tersebut dalam kondisi normal? 
 Soal 2. Berapa volume (no.) udara yang diperlukan untuk membakar 1 kg heptana?
Soal 2. Berapa volume (no.) udara yang diperlukan untuk membakar 1 kg heptana? 
Tugas 3. Hitung berapa volume (dalam l) dan berapa massa (dalam kg) karbon monoksida (IV) yang akan diperoleh dari pembakaran 5 mol oktan (no.). 
MEREKA. KHARCHEV
Manual pendidikan dan metodologi
Oleh kimia organik
kelas 10
Kelanjutan. Lihat Nomor 18, 19, 22/2006
Topik 5.
Sumber alami hidrokarbon
Ketahui: komposisi dan kegunaan alami dan terkait gas minyak bumi; komposisi dan sifat minyak; produk yang berasal dari minyak bumi; metode penyulingan minyak; penggunaan produk minyak bumi; metode pengolahan batubara; komposisi dan penggunaan produk kokas.
Mampu: membandingkan komposisi gas alam dan gas ikutannya; bandingkan komposisi dan sifat bensin yang diperoleh distilasi langsung, perengkahan katalitik dan perengkahan termal; buatlah persamaan reaksi yang terjadi selama cracking dan reforming.
Konsep dasar: distilasi fraksional, angka oktan, pirolisis, perengkahan katalitik dan termal, reforming, kokas.
Algoritma 5.1. Retaknya alkana linier
Latihan. Buatlah dua skema perengkahan untuk hidrokarbon linier n-oktan n-C 8 jam 18.
1. Cracking adalah pemecahan molekul alkana linier panjang menjadi molekul yang lebih pendek (sepanjang rantai karbon). Prosesnya berlangsung pada suhu 450–550 °C dengan adanya katalis atau tanpa katalis. Biasanya, rantai karbon putus kira-kira di tengah.
2. Dari satu molekul alkana diperoleh dua molekul yang lebih kecil - alkana dan alkena. Untuk alkana
N-C 8 H 18 mari kita buat dua skema cracking:
3. Persamaan reaksi dengan rumus struktur zat yang tertulis berbentuk:
n-S 8 N 18 N-C 4 H 10 + CH 2 = CHSN 2 CH 3,
n-S 8 N 18 N-C 5 H 12 + CH 2 = CHCH 3.
Algoritma 5.2. Reformasi hidrokarbon
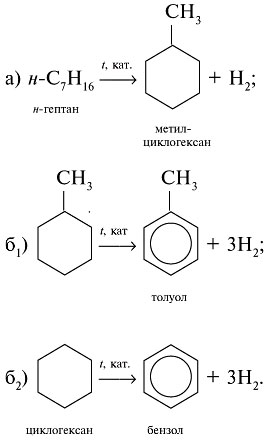
Latihan. Menyusun skema reformasi n-heptana N-C 7 N 16 dan sikloheksana siklo-C 6 jam 12.
1. Reformasi, atau aromatisasi minyak, adalah reaksi kimia selama pirolisis minyak, yang menghasilkan hidrokarbon dengan cincin benzena (arena).
2. Proses utama selama reforming adalah siklisasi alkana menjadi turunan sikloheksana (a) dan dehidrogenasi cincin jenuh menjadi cincin benzena (b):
Pertanyaan kontrol
1. Apa saja sumber hidrokarbon alami?
2. Apa komposisi gas alam dan gas terkaitnya?
3. Area penerapan gas alam.
4. Produk apa yang dapat diperoleh dari gas alam dan gas minyak bumi terkait? Apa kegunaannya?
5. Apa komposisi minyaknya?
6. Apa saja metode penyulingan minyak industri?
7. Sebutkan produk minyak bumi ringan. Dimana mereka digunakan?
8 . Apa perbedaan perengkahan termal dan katalitik ditinjau dari kondisi reaksi dan produk yang terbentuk?
9. Apa itu reformasi? Untuk tujuan apa hal itu dilakukan?
10. Apa komposisi batubara?
11. Sebutkan fraksi kokasnya.
12 . Sebutkan produk produksi kokas dan penerapannya.
13. Keamanan lingkungan selama penyulingan minyak.
Tugas pengendalian diri
1. Buat dua skema cracking N-heptan N-C 7 H 16 dengan pembentukan alkana dan alkena.
2. Tulis skema reformasi N-oktan N-C 8 H 18, di mana arena terbentuk - etilbenzena dan
1,2-dimetilbenzena (dengan abstraksi hidrogen).
Topik 6. Alkohol dan fenol
Ketahuilah: gugus fungsi alkohol; formula umum alkohol; klasifikasi alkohol; struktur alkohol monohidrat jenuh; penyebab terjadinya ikatan hidrogen pada alkohol dan pengaruhnya terhadap properti fisik; jenis isomerisme dan tata nama alkohol; sifat kimia alkohol monohidrat dan polihidrat, metode pembuatan dan penggunaannya; struktur fenol; klasifikasi fenol; isomerisme fenol; perbedaan antara fenol dan alkohol aromatik; sifat kimia, produksi dan penggunaan fenol; reaksi kualitatif terhadap fenol.
Mampu: menjelaskan pengaruh ikatan hidrogen pada alkohol terhadap sifat fisiknya; buatlah rumus struktur isomer alkohol dan beri nama; menyusun persamaan reaksi yang mencirikan sifat kimia dan produksi alkohol monohidrat, polihidrat, aromatik, dan fenol; menjelaskan pengaruh timbal balik atom-atom dalam molekul fenol dan ketergantungan sifat asam alkohol dan fenol pada strukturnya.
Konsep dasar: gugus fungsi, alkohol primer, sekunder dan tersier, ikatan hidrogen, diol, triol, eter dan ester, esterifikasi, alkohol aromatik, polikondensasi.
Algoritma 6.1. Isomerisme dan tata nama
alkohol monohidrat jenuh
Latihan 1. Sebutkan senyawa-senyawa berikut dengan menggunakan tata nama sistematik:

CONTOH).
1. Pilih rantai karbon terpanjang dan beri nomor dari ujung yang paling dekat dengan gugus hidroksi OH:

2. Tunjukkan dengan angka posisi akar (3-),
sebutkan radikalnya (metil),
sebutkan hidrokarbon rantai utama dengan penambahan akhiran “-ol” (butanol),
perhatikan posisi gugus hidroksi (-2),
tuliskan nama lengkapnya: 3-metilbutanol-2.
Contoh b).
1. Beri nomor rantai karbon dari gugus hidroksi:
![]()
2. Tunjukkan dengan nomor posisi substituen (2-),
beri nama substituen (klorin),
sebutkan alkohol tanpa substituen (propanol),
perhatikan posisi gugus hidroksi (-1),
tuliskan nama lengkapnya: 2-kloropropanol-1.
Contoh c).
1. Beri nomor pada rantai karbon pada kedua sisinya:

2. Sebutkan alkana yang sesuai dengan rantai karbonnya (pentana),
tulis sufiks yang menunjukkan adanya dua gugus hidroksi (diol) dalam senyawa,
menunjukkan posisi gugus hidroksi (-2,4),
tuliskan nama lengkapnya : pentanediol-2,4.
Contoh).
1. Beri nomor pada rantai karbon terpanjang dari ujung yang paling dekat dengan gugus hidroksi:

2. Tunjukkan dalam angka kedudukan radikal (2,5-), catat nomor dan nama radikal (dimetil),
sebutkan alkohol rantai utama (heptanol),
menunjukkan posisi gugus hidroksi (-3),
tuliskan nama lengkapnya: 2,5-dimetilheptanol-3.
Tugas 2. Tuliskan rumus isomer untuk 2,3-dimetilbutanol-2 dan beri nama zat tersebut.
1. Buatlah formula awal alkohol berdasarkan namanya:

2. Buatlah rumus isomer posisi gugus hidroksi:

3. Buatlah rumus isomer struktur:
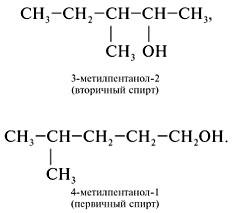
4. Buatlah rumus isomer dari kelas lain - eter. Alkohol monohidrat jenuh dan eter memiliki komposisi yang sama DENGAN N jam 2 N+2 O dan merupakan isomer:C
Algoritma 6.2. Sifat kimia dan produksi alkohol
Latihan 1. Tuliskan skema pembuatan isopropil alkohol dari 1-kloropropana dan persamaan reaksinya sesuai skema.
1. Buatlah diagram transformasi:

2. Buatlah persamaan reaksi menurut skema yang menunjukkan kondisi aliran dan jenis reaksi.
1) Hidrolisis basa:

2) Dehidrasi intramolekul:

3) Hidrasi:

Tugas 2. Bandingkan sifat asam etanol dan fenol.
1. Tuliskan rumus zat-zat berikut:

2. Kesamaan sifat asam - interaksi dengan logam alkali:
2C 2 H 5 OH + 2Na 2C 2 H 5 ONa + H 2,
2C 6 H 5 OH + 2Na 2C 6 H 5 ONa + H 2.
3. Perbedaan sifat asam - fenol menunjukkan sifat asam lebih jelas, tidak hanya berinteraksi dengan natrium, tetapi juga dengan natrium hidroksida:
C 6 H 5 OH + NaOH C 6 H 5 ONa + H 2 O.
Algoritma 6.3. Memecahkan masalah perhitungan
pada topik "Alkohol dan fenol"
Tugas 1. Tentukan massa aldehida yang terbentuk selama oksidasi etanol (hasil 75% dari hasil teoritis), jika diketahui bahwa ketika alkohol dalam jumlah yang sama bereaksi dengan natrium logam, 5,6 liter (n.s.) hidrogen dilepaskan.
1. Tuliskan kondisi permasalahannya.
V(H 2) = 5,6 liter,
(CH 3 ANAK) = 75%.
Menemukan:
M(CH 3 ANAK).
2. Tuliskan persamaan reaksi alkohol dengan natrium dan tentukan jumlah zat alkohol (C 2 H 5 OH):

3. Tuliskan persamaan oksidasi etanol dan tentukan massa teoritis aldehida M teori:
m teoritis = 22 g.
4. Temukan massa praktis aldehida:
= M praktis / M teori,
m latihan (CH 3 CHO) = 0,75 22 = 16,5 g.
Menjawab. M(CH 3 CHO) = 16,5 gram.
Tugas 2. Campuran etil dan propil alkohol seberat 16,6 g diolah dengan natrium berlebih, dan 3,36 l (n.s.) hidrogen dilepaskan. Tentukan fraksi massa alkohol dalam campuran.
1. Tuliskan kondisi permasalahannya.
campuran C 2 H 5 OH dan C 3 H 7 OH,
m(campuran) = 16,6 gram,
V(H 2) = 3,36 liter.
Menemukan:
(C 2 H 5 OH),
(C 3 H 7 OH).
2. Masukkan notasi:
m(C 2 H 5 OH) = X G,
M(C 3 H 7 OH) = kamu G.
Buat persamaan reaksi:

V 1 = 22,4 X/(2 46),
V 2 = 22,4 kamu/(2 60).
3. Buatlah sistem persamaan dan selesaikan:
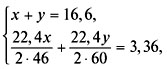

4. Temukan fraksi massa alkohol dalam campuran:
(C 2 H 5 OH) = 4,57/16,6 = 0,275, atau 27,5%,
(C 3 H 7 OH) = 72,5%.
Menjawab. (C 2 H 5 OH) = 27,5%, (C 3 H 7 OH) = 72,5%.
Pertanyaan kontrol
1. Zat apa yang disebut alkohol?
2. Apa itu rumus umum: a) alkohol monohidrat jenuh; b) alkohol polihidrat;
c) fenol?
3. Berikan contoh berbagai klasifikasi alkohol.
4. Jenis isomerisme apa yang menjadi ciri: a) alkohol monohidrat jenuh; b) alkohol polihidrat; c) fenol?
5. Bagaimana algoritma penyusunan nama alkohol?
6. Jenis ikatan kimia apa yang terdapat pada alkohol?
7. Apa penyebab terjadinya ikatan hidrogen pada alkohol dan apa pengaruhnya terhadap sifat fisik alkohol?
8. Apa sifat kimia dari: a) alkohol monohidrat jenuh; b) alkohol polihidrat;
c) fenol?
9. Apa persamaan dan perbedaan sifat kimia dari: a) alkohol monohidrat dan polihidrat;
b) alkohol monohidrat dan fenol; c) benzena dan fenol?
10. Apa persamaan dan perbedaannya (struktur dan sifat kimia) fenol dan alkohol aromatik?
11. Apa reaksi kualitatif terhadap: a) alkohol polihidrat; b) fenol?
12. Bagaimana cara memperolehnya: a) alkohol; b) fenol?
13. Jelaskan apa yang dimaksud dengan: alkohol primer (sekunder, tersier), ikatan hidrogen, reaksi esterifikasi, reaksi polikondensasi, diol (triol), eter, ester, alkohol aromatik.
Tugas pengendalian diri
1. Buatlah rumus struktur alkohol tersier yang mengandung 7 atom karbon dan beri nama senyawanya.
2. Buatlah rumus fenol diatomik isomer dan beri nama zatnya.
3. Buatlah persamaan reaksi yang mencirikan dualitas sifat alkohol:
Etana
13. Ketika 12 g alkohol monohidrat jenuh dipanaskan dengan asam sulfat, sebuah alkena ditimbang
6,3 g Hasil produk 75%. Tentukan rumus alkohol. Berapa banyak alkohol isomer yang sesuai dengan komposisi ini?
Menjawab. C 3 H 7 OH – propanol, 2 isomer.
Bersambung
1. Tuliskan rumus struktur hidrokarbon yang terdapat pada minyak dan mengandung 5 atom karbon per molekul.
2. Semua jenis bensin penerbangan mulai disuling pada suhu sekitar 40 0 C dan berakhir pada suhu praktis tidak lebih tinggi dari 180 0 C. Sebutkan hidrokarbon yang mengandung homolog metana: a) dengan yang paling rendah; b) dengan berat molekul relatif tertinggi.
3. Mengapa seringkali lebih sulit untuk mengisolasi masing-masing hidrokarbon dari fraksi minyak yang memiliki titik didih lebih tinggi daripada memperolehnya dari fraksi yang memiliki titik didih rendah? Yang metode kimia digunakan untuk mendaur ulang minyak?
4. Perlu dibuat larutan brom dalam bensin dengan kandungan brom yang tidak berubah selama penyimpanan. Haruskah saya menggunakan bensin lurus atau bensin retak untuk ini?
5. Apakah mungkin untuk membayangkan persamaan kimia proses yang terjadi: a) selama penyulingan minyak; b) selama perengkahan minyak. Berikan jawaban yang masuk akal.
6. Gas perengkahan minyak bumi manakah yang digunakan untuk memproduksi isopropil alkohol?
7. Apa perbedaan komposisi gas dari perengkahan termal dan katalitik? Untuk tujuan apa gas-gas ini digunakan?
8. Apa yang dimaksud dengan aromatisasi minyak? Tulis persamaan reaksi yang menjelaskan proses ini.
9. Berapakah angka oktan? Apakah struktur hidrokarbon mempengaruhi nilai bilangan ini? Apakah mungkin untuk meningkatkan angka oktan bensin yang diperoleh dengan menyuling minyak?
10. Jelaskan bensin yang diperoleh melalui perengkahan termal dan katalitik.
11. Tunjukkan nama produk minyak bumi yang paling penting dan buat daftar area penerapannya.
12. Apa bedanya cracking dengan pirolisis? Apa itu reformasi katalitik?
13. Berikan argumen geologi dan geokimia yang mendukung teori organik tentang asal usul minyak.
14. Minyak bumi yang dipecah menghasilkan etilen, yang dapat digunakan untuk menghasilkan asam asetat. Berikan persamaan untuk reaksi yang sesuai.
15. Hitung volume (no.) oksigen yang diperlukan untuk membakar 60 kg bensin yang mengandung 80% isomer heptana dan 20% isomer oktan.
16. Tuliskan persamaan reaksi yang dapat terjadi dengan hidrokarbon dodekana C 12 H 26 selama perengkahan minyak.
17. Apa itu kokas minyak bumi? Dari apa terbentuknya? Untuk apa ini digunakan? Berikan jawaban yang komprehensif.
18. Proses utama yang terjadi selama aromatisasi minyak (catalytic reforming) adalah dehidrogenasi nafta dan siklisasi alkana dengan dehidrogenasi secara simultan. Buatlah skema pembentukan metode-metode ini: a) benzena; b) toluena.
19. Hitung panas spesifik pembakaran gas sintesis yang terdiri dari 0,5 fraksi mol CO dan 0,5 fraksi mol H2, pada kondisi standar dan 298 0 K.
20. Hitung efek termal standar, konstanta kesetimbangan reaksi produksi metanol dari H 2 dan CO pada 298 0 K. Tentukan suhu di mana kesetimbangan reaksi ini terjadi pada kondisi standar.
Aromatisasi minyak
Aromatisasi minyak (minyak bumi)
Proses penyulingan minyak secara kimia, yang tujuan utamanya adalah memperolehnya aromatik hidrokarbon, terutama benzena, toluena, naftalena.
Buku referensi elektronik singkat tentang istilah-istilah dasar minyak dan gas dengan sistem referensi silang. - M.: Rusia Universitas Negeri minyak dan gas dinamai menurut namanya. I.M.Gubkina. MA. Mokhov, L.V. Igrevsky, E.S. pemula. 2004 .
Lihat apa itu “Aromatisasi minyak” di kamus lain:
AROMATISASI MINYAK- kimia. penyulingan minyak guna meningkatkan kandungan aromatik di dalamnya. hidrokarbon (turunan benzena). Sebuah. meningkatkan anti-ketukan St Va bahan bakar motor diperoleh dari minyak, dan memungkinkan produksi aromatik. hidrokarbon untuk bahan kimia pelacur... ... Kamus Besar Ensiklopedis Politeknik
AROMATISASI- (Latin baru, dari bahasa Yunani aroma dupa). Memberi suatu bau dengan menggunakan zat yang harum. Kamus kata-kata asing, termasuk dalam bahasa Rusia. Chudinov A.N., 1910. AROMATISASI novolat., dari bahasa Yunani. aroma, dupa. Menambah aroma...... Kamus kata-kata asing dari bahasa Rusia
AROMATISASI PRODUK MINYAK- pengolahan kimianya untuk meningkatkan kandungan hidrokarbon aromatik. Hal ini paling sering dilakukan dengan reformasi katalitik fraksi nafta minyak bumi. Dengan mengaromatisasi produk minyak bumi, bensin beroktan tinggi diperoleh... ... Kamus Ensiklopedis Besar
aromatisasi produk minyak bumi- pengolahan kimianya untuk meningkatkan kandungan hidrokarbon aromatik. Hal ini paling sering dilakukan dengan reformasi katalitik fraksi nafta minyak bumi. Dengan mengaromatisasi produk minyak bumi, beroktan tinggi... ... kamus ensiklopedis
Penyedap produk minyak bumi- pengolahan kimia produk minyak bumi untuk meningkatkan kandungan hidrokarbon aromatik di dalamnya (Lihat Hidrokarbon aromatik) dengan mengubah hidrokarbon rantai terbuka menjadi hidrokarbon siklik. Sebuah.... ... Ensiklopedia Besar Soviet
Penyulingan minyak- Kilang minyak shell di California Tujuan penyulingan minyak (oil refining) adalah produksi produk minyak bumi ... Wikipedia
Kazansky, Boris Alexandrovich- Kazansky Boris Aleksandrovich ... Ensiklopedia Investor Wikipedia













